Eindeutige Kennzeichnung von Arzneimitteln
Das GS1 System wird in der Schweiz seit über 30 Jahren zur Identifikation und Auszeichnung von Arzneimitteln eingesetzt. Bis heute konnte eine fast 100-prozentige Abdeckung der Swissmedic zugelassenen Arzneimitteln erreicht werden.
Die Identifikation und Auszeichnung von Arzneimitteln über alle Verpackungsstufen sind einer der Grundpfeiler zur Digitalisierung von Medikationsprozessen. Sie ermöglichen Anwendungen wie das Bundesgesetz über das Elektronische Patienten Dossier, den elektronischen Impfausweis und die Digitalisierung von Supply Chain und Klinikprozessen.
Identifikation als Mehrwert
Die Informationen werden mittels Barcode direkt auf der jeweiligen Verpackungsstufe aufgedruckt und stehen allen Anwendern entlang der Supply Chain und des klinischen Patientenpfades zur Verfügung. Durch den direkten Aufdruck der Identifikationsschlüssel sowie zugehöriger Attribute auf der Verpackung wird ein grosser Mehrwert generiert. So können diese Informationen an jeder Station der Supply Chain und des klinischen Patientenpfades unmittelbar erfasst und in die IT-Systeme übernommen werden.
Eindeutigkeit erhöht Sicherheit
Durch die weltweite Eindeutigkeit der Identifikationsschlüssel werden, im Gegensatz zu proprietären Identifikationen, Fehler ausgeschlossen. Gleichzeitig werden die Patientensicherheit erhöht und Supply Chain Prozesse effizienter gestaltet.
Einigung auf einheitlichen Standard
In der Schweiz haben sich die Stakeholder vor gut 30 Jahren darauf verständigt, dass Arzneimittel unter Anwendung des GS1 Systems mit einer Global Trade Item Number (GTIN) ausgezeichnet werden. Zwischenzeitlich haben sich weltweit die meisten Länder für den Einsatz des GS1 Systems zur Identifikation von Arzneimitteln entschieden.

Grundlagen zur Identifikation und Auszeichnung von Arzneimitteln
Verpackungsstufen von Arzneimitteln und deren Auszeichnung
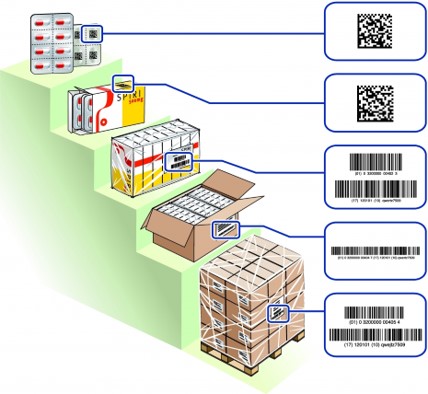
- Primärverpackung
- Sekundärverpackung
- Tertiärverpackung (z.B. Bündelpackung)
- Quartärverpackung (z.B. Karton und/oder Paletten)
| Verpackungsstufe | Produkteidentifikation | GS1 Barcode Typ |
|---|---|---|
| Primärverpackung | GTIN A, wie 0 76 12345 00253 x |
GS1 DataMatrix |
| Sekundärverpackung | GTIN B, wie 0 7680 12345 678 x |
GS1 DataMatrix und/oder EAN-13 |
| Tertiärverpackung (Multipack/Spitalpackung) | GTIN C, wie 0 76 12345 00254 x |
GS1-128 |
| Quartärverpackungen (Karton und/oder Paletten) |
GTIN D, wie 0 76 12345 00255 x |
GS1-128 |
Informationen zur Auszeichnung von Primärverpackungen
Primärverpackungen werden mit einem GS1 DataMatrix ausgezeichnet, der als Minimalinformation die GTIN (Produktidentifikation) und Lot enthält und im Idealfall auch das Verfalldatum. Welche Informationen im GS1 DataMatrix verschlüsselt werden, ist vom zur Verfügung stehenden Platz abhängig. Wenn möglich sollten alle Informationen im Barcode enthalten sein, jedoch hat der Dateninhalt direkte Auswirkungen auf die Barcodegrösse. Auf die HRI (Human Readable Interpretation oder Klarschrift Zeile) kann bei der Primärverpackung verzichtet werden, wenn dies aus Platzgründen nicht möglich ist. Die Auszeichnung der Primärverpackung ist die Grundlage für die Digitalisierung des Medikationsprozesses und des Bed Side Scanning Prozesses im klinischen Patientenpfad.
Informationen zur Auszeichnung von Sekundärverpackungen
Sekundärverpackungen werden mit einem GS1 DataMatrix ausgezeichnet, der die Informationen GTIN (Produktidentifikation), Lot und Verfalldatum enthält. Zukünftig werden im GS1 DataMatrix der Sekundärverpackung auch die eindeutige Serial-Nummer enthalten sein, die im Rahmen der Umsetzung der FMD (Falsified Medicine Directive) verlangt wird. Neben, unter oder über der GS1 DataMatrix ist jeweils eine HRI (Human Readable Interpretation oder Klarschrift Zeile) anzubringen, welche die eincodierten Werte aufzeigt. Da es heute noch keine Garantie gibt, dass alle POS Systeme in Apotheken und Drogerien einen 2-dimensionalen Barcode verarbeiten können, kann auf einer anderen Verpackungsseite noch zusätzlich ein EAN-13 Barcode angebracht werden. Damit wird sichergestellt, dass eine Erfassung des Barcodes auch mit älteren POS-Systemen möglich ist. Eine Auszeichnung der Verpackungen mit einem GS1 DataMatrix erlaubt es Attribute zum Produkt (Lot, EXP, Serial-Nr) mit dem Scanner einzulesen und dem nachgelagerten IT-System zur Verfügung zu stellen. Dies ermöglicht erweiterte Funktionen in POS-Systeme zu integrieren, wie z.B. die Kontrolle des Verfalldatums vor der Abgabe und auch die vollautomatische Einlagerung in einem Roboter.
Informationen zur Auszeichnung von Tertiärverpackungen
Tertiärverpackungen werden mit einem GS1-128 Barcode ausgezeichnet, der die Informationen GTIN (Produktidentifikation), Lot und Verfalldatum enthält. Neben, unter oder über dem GS1-128 Barcode ist jeweils eine HRI (Human Readable Interpretation oder Klarschrift Zeile) anzubringen, welche die verschlüsselten Werte aufzeigt. Für Tertiärverpackungen wir ein eindimensionales Symbol verwendet, weil davon auszugehen ist, dass solche Packungen durch ein automatisiertes Logistiksystem ein- und ausgelagert werden könnten, welches nicht zwingend ein zweidimensionales Symbol verarbeiten kann.
Informationen zur Auszeichnung von Quartärverpackungen
Quartärverpackungen werden mit einem GS1-128 Barcode ausgezeichnet, der die Informationen GTIN (Produktidentifikation), Lot und Verfalldatum enthält. Neben, unter oder über dem GS1-128 Barcode ist jeweils eine HRI (Human Readable Interpretation oder Klarschrift Zeile) anzubringen, welche die verschlüsselten Werte aufzeigt. Für Quartärverpackungen wir ein eindimensionales Symbol verwendet, weil davon auszugehen ist, dass solche Packungen durch ein automatisiertes Logistiksystem ein- und ausgelagert werden könnten, das nicht zwingend ein zweidimensionales Symbol verarbeiten kann.
Barcodes zur Auszeichnung von Arzneimitteln
Zur Auszeichnung von Arzneimitteln sollten in der Schweiz jeweils die drei nachfolgenden erläuterten Barcodes eingesetzt werden.
|
Barcode |
Dateninhalt | Bemerkungen |
Nur GTIN |
Kann von 1D und 2D Scannern gelesen werden Kann von allen Kassensystemen mit Scanner in Apotheken verarbeitet werden Anwendung auf Sekundärverpackungen |
|
|
(01)07612345002552 |
GTIN + Attribute [GS1 Application Identifier Standard] |
Kann nur von 2D Scannern gelesen werden Erlaubt das Auslesen von Informationen wie Lot, EXP und Serialnummer Anwendung auf Primär- und Sekundärverpackungen |
GTIN + Attribute [GS1 Application Identifier Standard] |
Kann von 1D und 2D Scannern gelesen werden Erlaubt das Auslesen von Informationen wie Lot, EXP und Serialnummer Anwendung auf Tertiär- und Quartärverpackungen
|
Was passiert im Hintergrund, wenn ein Barcode von einem Scanner gelesen wird?
Unser Erklärfilm "Einlesen eines Barcodes" zeigt, welche Aktion in einem IT-System ausgelöst wird, nachdem ein Barcode eingescannt wurde.

Identifikation von Arzneimitteln mit Swissmedic Zulassung
Für die Kennzeichnung von Arzneimitteln in der Schweiz ist eine Sonderlösung in Zusammenarbeit mit dem schweizerischen Heilmittelinstitut (Swissmedic) vereinbart worden. Sie fügt sich in den internationalen Standard ein und kann als solche auch für Exporte verwendet werden, sofern im Empfangsland keine anderslautenden Vorschriften für die Artikelnummerierung im Gesundheitswesen bestehen.
Die Zuteilung der GTIN erfolgt ausschliesslich für durch Swissmedic zugelassene Arzneimittel und immunbiologische Erzeugnisse mit 5-stelligen Zulassungsnummern und 3-stelligen Packungscodes.
Dieses Datenelement hat folgenden Aufbau:
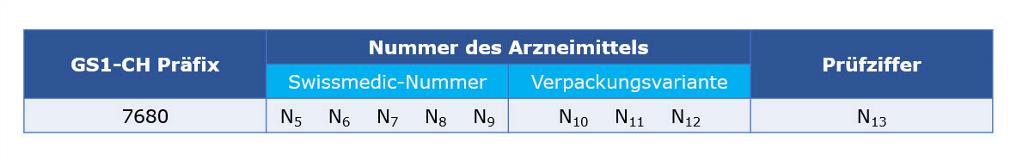
Hinweis:
Alle übrigen von Swissmedic zugelassenen Arzneimitteln müssen mit firmeneigenen GTINs identifiziert werden. Mehr Informationen finden Sie im Kapitel 9 Nationale Spezifikationen für die Schweiz der Allgemeinen GS1 Spezifikationen.
Es steht dem Zulassungsinhaber frei, diese nationale Lösung zur Identifikation und Auszeichnung von Arzneimitteln zu verwenden oder die Auszeichnung mit eigenen GTINs vorzunehmen. Diese Lösung wurde 1984 etabliert, um die Medikamentensicherheit und Prozesse in der Schweiz zu verbessern.
In der Schweiz zugelassene Arzneimittel sind zur Basisreferenzierung in der refdatabase einzutragen. www.refdata.ch
Weitere Infos
Auswirkungen durch die Umsetzung der FMD in der Schweiz
Zur Umsetzung der Falsified Medicine Directive (FMD) in der Schweiz wurde im Rahmen der Revision des Heilmittelgesetzes (HMG) eine Reihe von Massnahmen definiert. Die Vorgaben erfolgten von der Europäischen Union und dem Schweizer Bundesrat und zielen darauf ab, Patienten gegen gefälschte Arzneimittel in der legalen Lieferkette zu schützen. Die gesetzliche Grundlage dafür sind die Fälschungsschutzrichtline 2011/62/EU, die Delegierte Verordnung (EU) 2016/161 sowie der Art. 17a HMG und die damit verbundene Verordnung, Art. 17a HMG.
Diese neuen regulatorischen Vorgaben betreffen nur RX Medikamente, also Arzneimittel, die der Swissmedic Liste A und B zugeordnet sind.
Hinweis: Auswirkungen durch Corona
Wegen der Corona-Pandemie kann das BAG zurzeit keine verbindliche Aussage machen, wann die Verordnung zu Artikel Art. 17a HMG in Kraft tritt. Das BAG hat die Stellungnahmen zur entsprechenden Vernehmlassung veröffentlicht. Sie finden diese auf der Webseite des BAG zum Download.
Individuelle Erkennungsmerkmale in der Supply Chain
Die Konsequenzen aus dieser Massnahme sind individuelle Erkennungsmerkmale und Sicherheitsvorrichtungen auf der Verpackung von Arzneimitteln. Mehr Informationen zum Thema.
Als individuelles Erkennungsmerkmal dient eine pseudo-randomisierte Serialnummer auf jeder Sekundärverpackung, die mittels einem GS1 DataMatrix-Barcode und einer HRI (Human Readable Interpretation) auf der Packung aufgedruckt wird.
Parallel dazu wird ein Verifikationssystem aufgebaut, in das die Hersteller ihre Serialnummer-Informationen hochladen, bevor die Produkte in die Supply Chain kommen.
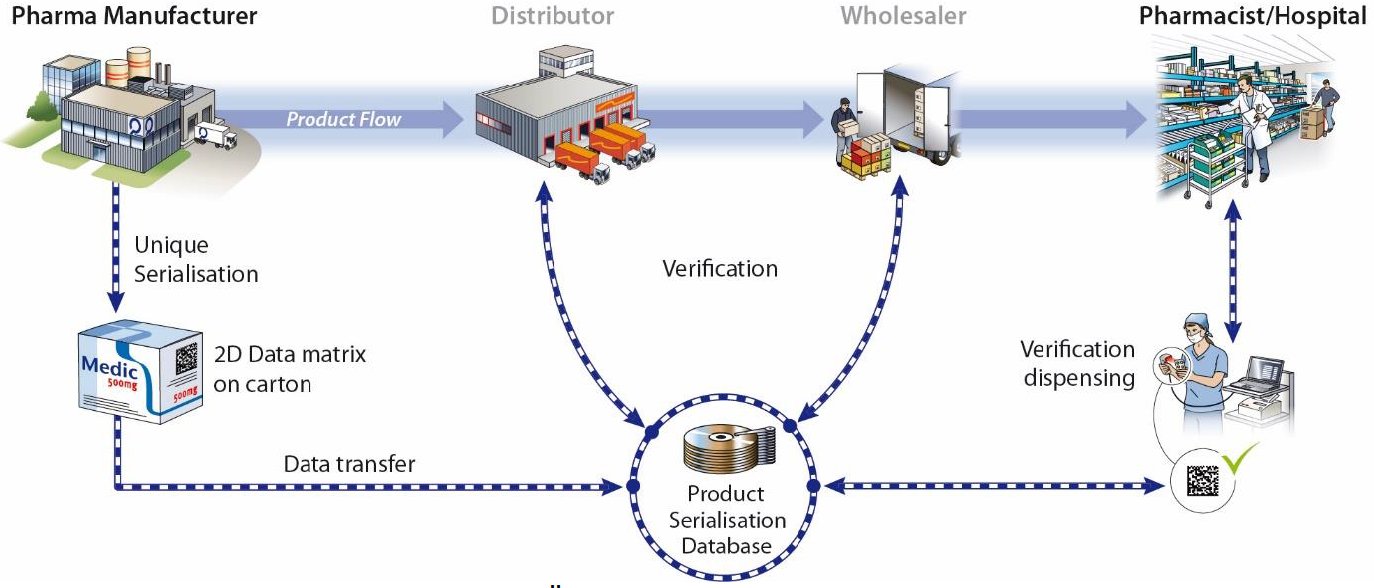
Bei der Abgabe in der Apotheke, im Spital oder beim Arzt, wird das Datenelement auf der Verpackung gegen das Verifikationssystem geprüft und die jeweilige Packung in der Datenbank als verbraucht gekennzeichnet. Dieses System erlaubt eine Prüfung bei allen Stationen des physischen Warenflusses und verhindert so die Penetration der ordentlichen Supply Chain mit gefälschten Produkten.
Zu den Sicherheitsvorrichtungen auf der Verpackung gehört insbesondere auch, dass zukünftig nur noch Verpackungen in den Verkehr gebracht werden dürfen, die «Tamper Proof» (Erstöffnungsgarantie) sind, d.h. eine Verpackung muss so gestaltet sein, dass diese nicht wieder verschlossen werden kann.
Das GS1 System erlaubt es die Medikations- und Patientensicherheit zu erhöhen, vereinfacht die Dokumentation in klinischen Informationssystemen und erhöht die Effizienz des klinischen Patientenpfades und der Supply Chain.
- Das GS1 System ist die Grundlage zur Digitalisierung des Gesundheitswesens.
- Mit den GS1 Identifikationsschlüsseln werden Arzneimittel, Patienten, Pflegefachleute und Lokationen eindeutig identifiziert.
- Mit GS1 Barcodes werden Identifikation und Attribute auf jedem Objekt in maschinen- und menschenlesbarer Form verfügbar gemacht.
- Mit dem Stammdatenaustausch Standard GDSN (Global Data Synchronisation Network), können Stammdaten über mehrere Parteien schnell und einfach ausgetauscht werden und es entfallen aufwändige Mappings.
- Der GS1 EDI Standard vereinfacht die Digitalisierung des Order-to-Cash Cycles.
Hinweis
Benötigen Sie einen Pharmacode?
Den Pharmacode erhalten Sie direkt bei HCI Solutions AG unter folgenden Koordinaten: www.hcisolutions.ch / Tel. 058 851 26 00